光纤布拉格光栅传感器:微创医疗的研究前沿与精准化实践
来源:传感诸葛孔明
发布时间:2025-09-26
在微创手术室中,外科医生的双手并不直接接触患者的内脏组织,而是操控着数米之外的机械臂完成切割、缝合、消融等精细操作。这种“遥操作”模式虽然减少了创伤,却带来了一个关键难题:医生失去了直接触摸组织所带来的力反馈和温度感知能力。这正是近年来光纤布拉格光栅传感器在微创医疗领域掀起技术变革的起点。
一、微创医疗的感知困境与FBG的破局之道
自1997年达芬奇手术机器人问世以来,机器人辅助微创手术系统快速发展。然而,触觉反馈缺失始终是技术提升的瓶颈。医生无法感知手术器械与组织间的相互作用力,难以判断组织硬度、血管搏动甚至异常肿块,这直接影响手术的精准度和安全性。
传统的电信号传感器(如压阻式、压电式传感器)虽然能够提供一定的力反馈,但在实际应用中存在明显局限:易受电磁干扰、体积较大、生物兼容性差,且在高湿度的外科环境中稳定性不足。而FBG传感器凭借其直径细小(与人体头发丝相当)、完全抗电磁干扰、本质安全等独特优势,成为微创手术器械理想的感知解决方案。
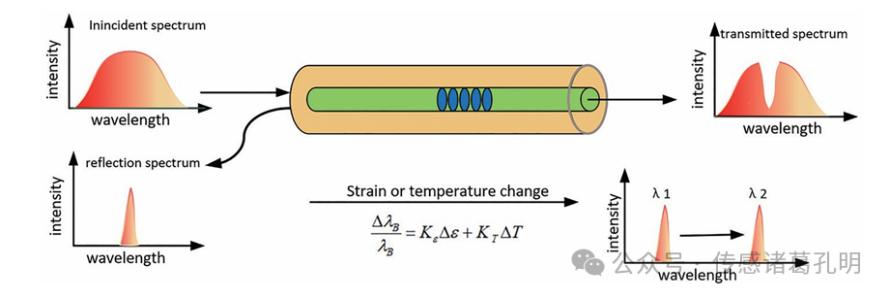
图1 FBG传感原理示意图:当外界力或温度变化时,反射光的特征波长会发生偏移
FBG的本质是在光纤纤芯内刻写的一段周期性折射率分布结构。当宽带光传入时,特定波长的光会被反射,其余光透射。这个反射波长会随着光纤所受应变或温度变化而发生线性偏移,通过监测波长位移量,即可高精度还原外界物理量变化。
二、力触觉感知:为手术器械装上“敏感指尖”
2.1 眼科手术:毫牛级精度的视网膜微钳
眼科手术对力的感知要求极为苛刻,不适当的力可能导致不可逆的视网膜损伤。约翰霍普金斯大学计算机辅助外科手术研究中心团队自2009年起持续创新,将FBG传感器嵌入直径不足1毫米的微型手术钳中,实现了从一维到三维力感知的跨越式发展。
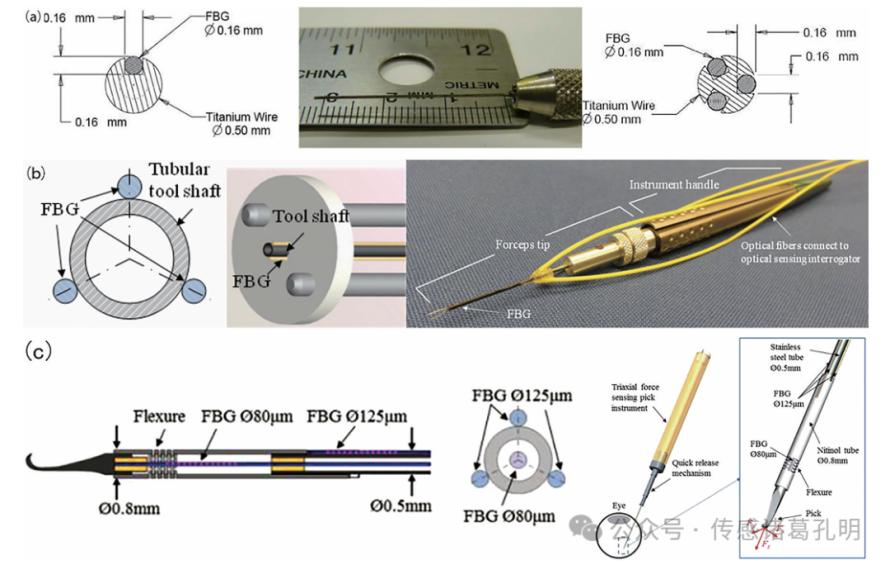
图2 用于视网膜手术的FBG力感知微钳结构演变
2.2 组织触诊:从心脏消融到肿瘤识别
在心脏射频消融手术中,导管与心组织的接触力过大易导致心脏穿孔。中国科学院沈阳自动化研究所开发的三维力传感导管,通过中心FBG测轴向力、周向三根FBG测径向力,实现了-100~100克范围内的精准力控。天津大学王树新团队则基于Sarrus机构设计出柔性铰链结构,使传感器在0~5牛的大范围内仍能保持2.55毫牛的高分辨率,可用于术中组织硬块的识别。
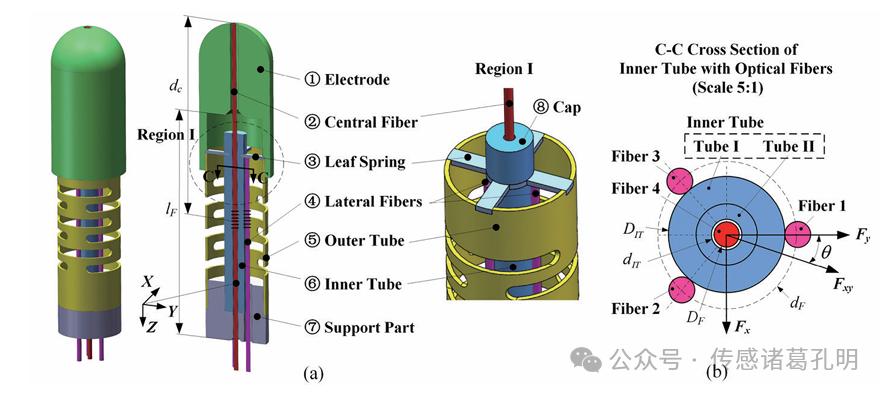
图3 用于心脏导管的三维力传感器结构
2.3 穿刺手术:实时追踪针形轨迹
在活检或药物注射穿刺过程中,针具易因组织不均质发生弯曲。哈佛大学团队将三根FBG以120度间隔布置在针身,通过波长变化反推针体弯曲曲率,生成实时针形轨迹图,帮助医生更精准地控制针具路径。
三、温度感知:为热消融治疗装上“火眼金睛”
肿瘤热消融治疗要求将组织温度精准控制在42~45℃之间:温度过低无法杀死癌细胞,过高则会损伤健康组织。FBG温度传感器正在这一领域发挥关键作用。
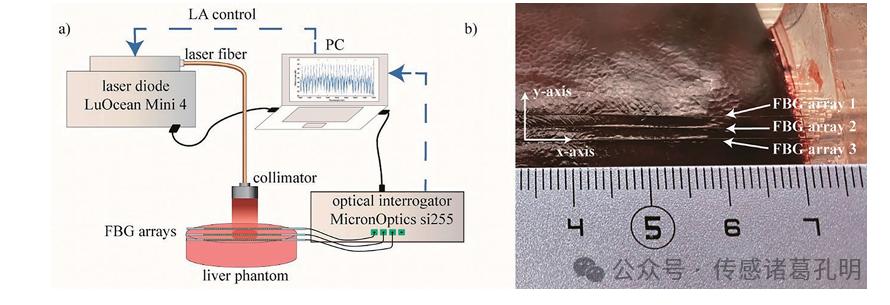
图4 基于FBG的肝组织激光消融温度控制系统
浙江大学团队开发的肿瘤消融监测系统,将多个FBG探针插入肝脏组织,成功监测了微秒/纳秒脉冲电场下的温度分布,温度分辨率达0.1℃,空间分辨率达2.5毫米,为精准消融提供了重要数据支持。
四、挑战与未来:从实验室走向手术室的必经之路
尽管FBG传感技术展现出巨大潜力,但其在临床推广应用仍面临三大挑战:
1.温度-力交叉敏感:手术环境中温度变化会干扰力测量结果,需开发有效的温度补偿和解耦算法。
2.多维力测量精度:同时检测轴向和横向力时精度下降,需要更优化的机械结构设计。
3.系统集成度:目前FBG传感系统仍相对独立,与手术机器人的信息融合和实时交互能力有待提升。
未来,随着飞秒激光光栅刻写技术的进步,更高密度、更强鲁棒性的FBG阵列将成为可能。结合人工智能算法,FBG传感器有望实现从“单点感知”到“全场感知”的跨越,最终构建智能医疗传感网络,为微创手术提供更全面、精准的实时反馈。
五、结语
光纤布拉格光栅传感器正以其独特的技术优势,悄然改变着微创医疗的感知维度。它不仅是手术器械的“敏感神经”,更是医生在微创世界中的“隐形触角”。随着技术的不断成熟和临床验证的深入,FBG传感技术有望在不久的将来成为高端微创手术机器的标准配置,为精准医疗提供坚实的技术支撑。
免责声明
- 1、本文内容版权归属原作者、原发表出处。若版权所有方对本文的引用持有异议,请联系感算商城(service@gansuan.com),我方将及时处理。
- 2、本文的引用仅供读者交流学习使用,不涉及商业目的。
- 3、本文内容仅代表作者观点,感算商城不对内容的准确性、可靠性或完整性提供明示或暗示的保证。读者阅读本文后做出的决定或行为,是基于自主意愿和独立判断做出的,请读者明确相关结果。
- 4、如需转载本方拥有版权的文章,请联系感算商城(service@gansuan.com)注明“转载原因”。未经允许私自转载感算商城将保留追究其法律责任的权利。







